El tratamiento que podrĻŠa reducir en un 85% la mortalidad de la COVID
La Agencia Europea del medicamento estĻĒ revisando el uso del anticuerpo monoclonal VIR-7831 para tratar a pacientes con riesgo de padecer un cuadro grave.
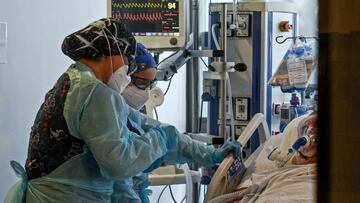
La Agencia Europea del Medicamento (EMA) estĻĒ revisando los datos sobre el uso del anticuerpo monoclonal VIR-7831, de las compa?ĻŠas GSK y Vir Biotechnology, para el tratamiento de pacientes con COVID-19. SegĻēn explica la agencia en un comunicado, la revisiĻŪn incluirĻĒ datos de un estudio que compara el efecto de VIR-7831 con el placebo en pacientes adultos y adolescentes (mayores de 12 a?os y que pesen al menos 40 kg) con COVID-19 de leve a moderada que tenĻŠan un alto riesgo de progresar a un diagnĻŪstico mĻĒs grave.
El ComitĻĶ de Medicamentos de Uso Humano (CHMP) de la EMA examinarĻĒ la eficacia del medicamento para prevenir la hospitalizaciĻŪn y la muerte en pacientes con COVID-19 no hospitalizados que no requieren suplemento de oxĻŠgeno. Los resultados preliminares indican que VIR-7831 redujo el riesgo de hospitalizaciĻŪn durante mĻĒs de 24 horas o de muerte en un 85% en comparaciĻŪn con el placebo. El CHMP tambiĻĶn evaluarĻĒ los datos sobre la calidad y la seguridad del medicamento.
Aunque la EMA prevĻĶ que se inicie una revisiĻŪn continua mĻĒs exhaustiva antes de una posible solicitud de autorizaciĻŪn de comercializaciĻŪn, la revisiĻŪn actual proporcionarĻĒ recomendaciones a nivel de la UniĻŪn Europea (UE) para las autoridades nacionales que pueden tomar decisiones basadas en la evidencia sobre el uso temprano del medicamento.
QuĻĶ son y cĻŪmo funcionan los anticuerpos monoclonales
De acuerdo con la EMA, el VIR-7831 (GSK4182136) es un anticuerpo monoclonal con actividad contra el SARS-CoV-2, el virus que causa la COVID-19. Ą°Un anticuerpo monoclonal es un tipo de proteĻŠna que se adhiere a una estructura especĻŠfica (llamada antĻŠgeno)Ąą, a?ade.
De esta forma, el VIR-7831 estĻĒ dise?ado para unirse a la proteĻŠna de pico del SARS-CoV-2, lo que limita la capacidad del virus para ingresar a las cĻĶlulas del cuerpo. Ą°Los datos preclĻŠnicos sugieren que tiene el potencial de bloquear la entrada del virus en las cĻĶlulas sanas y eliminar las cĻĶlulas infectadasĄą, se?ala en su pĻĒgina web Vir Biotechnology. AdemĻĒs, la empresa habla sobre VIR-7832 (GSK4182137), otro anticuerpo monoclonal. Peso este es de doble acciĻŪn, con lo que tiene una mayor capacidad para eliminar las cĻĶlulas infectadas.
AdemĻĒs, datos preclĻŠnicos adicionales publicados en bioRxiv revelan que Ą°el VIR-7831 mantiene la actividad contra las variantes de interĻĶs que circulan actualmenteĄą, incluidas la britĻĒnica, sudafricana brasile?a y californiana.
No se puede comercializar
Esta semana, la AdministraciĻŪn Australiana de Productos TerapĻĶuticos (TGA), otorgĻŪ a VIR-7831 una determinaciĻŪn provisional. Se trata del primer anticuerpo monoclonal anti-SARS-CoV-2 al que se le ha otorgado esta designaciĻŪn, que proporciona un mecanismo formal y transparente para acelerar el registro de nuevos medicamentos prometedores con datos clĻŠnicos preliminares.
Eso sĻŠ, es un compuesto en investigaciĻŪn y no se le ha otorgado una autorizaciĻŪn de comercializaciĻŪn en ningĻēn lugar del mundo, aunque ya se ha enviado una solicitud de AutorizaciĻŪn de Uso de Emergencia a la FDA de Estados Unidos.